Химические свойства бутана уравнения. изобутан: формула, свойства, применение
Содержание:
Область применения пропан-бутана

Смесь пропана и бутана широко применяется в качестве альтернативного вида топлива для систем газоснабжения частных домов, небольших предприятий, промышленных помещений и крупных производственных комплексов. По сравнению с природным газом пропан-бутан имеет ряд преимуществ и особенностей эксплуатации, которые подробно рассматривались в статье «Химические и физические свойства СУГ».
Кроме применения в качестве топлива пропан и бутан могут встречаться:
- На этапе резки металла Смешение ацетилена, пропана или пропан-бутана с кислородом создает горячую пламенную струю, которая дает возможность разогреть поверхность металла до температуры начала горения. При подаче кислорода происходит воспламенение в месте соприкосновения с металлом и выполняется резка нужной формы.
- При выполнении сварочных работ Горелки для ручной газовой сварки низкоуглеродистых сталей, пайки и наплавки цветных металлов, а также для различного сортамента сталей работают на пропан-бутановой смеси.
- В пищевой промышленности Пищевые добавки Е944 и Е943а применяются в качестве пропеллентов. Е944 (пропан) помогает уменьшить концентрацию ароматизаторов готового продукта и используется как растворитель жирных кислот, что дает возможность получить ряд низкокалорийных продуктов. Е943а (бутан) дает возможность выдавить из баллонов растительные сливки, муссы, пищевые красители т.д.
- В системе охлаждения Пропан и изобутан могут выступать в роли хладагентов для кондиционеров и холодильных установок.
- На витринах художественных магазинов Аэрозольные баллончики с краской заправляются смесью пропан-бутана вместо воздуха. Воздух создает высокое давление внутри баллона, а легко сжижающийся газ позволяет обеспечить равновесное состояние жидкости и газа. При нажатии на клапан краска распыляется под давлением.
- В транспортной отрасли Вещество используется как топливо не только для систем газоснабжения домов, но и как чистое топливо для двигателей внутреннего сгорания.
- В косметических средствах Производители косметики выпускают множество продуктов в виде спреев, муссов и аэрозолей — это дезодоранты, средства для укрепления волос, солнцезащитный крем, крем для загара и т.д. Пропан-бутан используется опять же в качестве пропеллента для распыления средства на кожу тонким равномерным слоем.
Хранение пропан-бутана осуществляется в специальных стальных газгольдерах под давлением 1,6 МПа. Конструктивно газгольдеры представляют собой стальные сосуды цилиндрической формы с эллиптическими или торосферическими днищами, которые могут устанавливаться наземно или подземно.

Реакции
Спектр синего пламени от бутановая горелка показывая CH молекулярный радикальный полосы излучения и C2Лебединые группы
Когда кислорода много, бутан горит с образованием углекислый газ и водяной пар; когда кислород ограничен, углерод (сажа) или монооксид углерода. Бутан плотнее воздуха.
Когда кислорода достаточно:
- 2 С4ЧАС10 + 13 O2 → 8 СО2 + 10 часов2О
Когда кислород ограничен:
- 2 С4ЧАС10 + 9 O2 → 8 СО + 10 ч2О
Максимум адиабатическое пламя температура бутана с воздуха составляет 2243 К (1970 ° C; 3578 ° F).
п-Бутан — сырье для DuPontкаталитический процесс приготовления малеиновый ангидрид:
- 2 канала3CH2CH2CH3 + 7 O2 → 2 С2ЧАС2(CO)2O + 8 H2О
п-Бутан, как и все углеводороды, подвергается свободный радикал хлорирование дает как 1-хлор-, так и 2-хлорбутаны, а также более сильно хлорированные производные. Относительные скорости хлорирования частично объясняются разными энергии диссоциации связи, 425 и 411 кДж/ моль для двух типов связей C-H.
Технические характеристики
На вопрос: «Каким образом химические и физические свойства связаны с техническими особенностями этой смеси?», стоит рассматривать все возможные варианты ответов.
- Во-первых, благодаря своему высокому давлению «удержания» в жидком состоянии, этот газ слишком инертный. То есть легко поддается переходу из жидкого состояния в газообразное.Это очень полезная особенность на производствах, где это является крайней необходимостью.
- Во-вторых, низкая температура кипения и замерзания делает пропан-бутановую смесь стойкой к «столкновениям» с веществами азотного происхождения. Следовательно, гарантирует ей безопасность от замерзания и кипения.
- Ну и, конечно же, стоит отметить высокую температуру горения пропана, без которой его польза была бы не столь существенной для достижения определенных бытовых или производственных целей.
История вопроса
Благодаря хорошим характеристикам хладагент R600a (HC 600a) использовался в холодильниках с начала 20 века. После появления хладагента R12, изобутан перестали использовать из-за того, что его требовалось много, 200-400 грамм в одном бытовом холодильнике.
В больших объемах хладон r600a был пожароопасным в таких количествах. В случае утечки он мог воспламениться от открытого огня, электрической искры и привести к пожару. На десятилетия изобутан был забыт.
В 20 веке холодильная техника постоянно совершенствовалась. К 1990 годам для работы системы бытового холодильника нужно было не более 150 грамм изобутана. К тому же, после подписания Монреальского протокола, хладагент R12 стали выводить из обращения. Фреон R600a стал основным хладагентом для бытовой холодильной и морозильной техники.
Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Бутан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании бутана образуется смесь хлорпроизводных.
|
Например, при хлорировании бутана образуются 1-хлорбутан и 2-хлорбутан:
CH3-CH2-CH2-CH3 + Cl2 → CH3-CH2-CH2-CH2Cl + HCl CH3-CH2-CH2-CH3 + Cl2 → CH3-CH2-CHCl-CH3 + HCl |
Бромирование протекает более медленно и избирательно.
|
Избирательность бромирования: сначала замещается атом водорода у третичного атома углерода, затем атом водорода у вторичного атома углерода, и только затем первичный атом.
С третичный–Н > С вторичный–Н > С первичный–Н |
|
Например, при бромировании пропана преимущественно образуется 2-бромбутан: CH3-CH2-CH2-CH3 + Br2 → CH3-CH2-CHBr-CH3 + HBr |
Хлорбутан может взаимодействовать с хлором и дальше с образованием дихлорбутана, трихлорбутана, тетрахлорбутана и т.д.
1.2. Нитрование бутана
Бутан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в бутане замещается на нитрогруппу NO2.
| Например. При нитровании бутана образуется преимущественно 2-нитробутана: |
CH3-CH2-CH2-CH3 + HNO3 → CH3-CH2-CHNO2-CH3 + H2O
Получение бутана. Химические реакции – уравнения получения бутана:
Так как бутан в достаточном количестве содержится в природном газе, попутном нефтяном газе и выделяется при крекинге нефтепродуктов, его не получают искусственно. Его выделяют при очистке и сепарации из природного газа , ПНГ и нефти при перегонке.
Бутан в лабораторных условиях получается в результате следующих химических реакций:
- 1. гидрирования непредельных углеводородов , например, бутена:
- 2. восстановления галогеналканов:
- 3. взаимодействия галогеналканов с металлическим щелочным металлом , например, натрием (реакция Вюрца):
Суть данной реакции в том, что две молекулы галогеналкана связываются в одну, реагируя с щелочным металлом .
- 4. щелочного плавления солей одноосновных органических кислот:
Сфера применения газа
Пропан-бутан представляет собой уникальное вещество на газовой основе, которое имеет в своем составе одноименные молекулы.
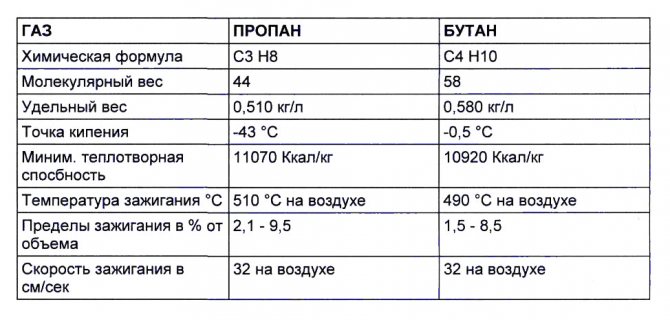
Общепризнанная химическая формула пропана состоит из молекул и атомов двух основных составляющих – пропана (С3Н8) и бутана (С4Н10).
Широко используемый в бытовых целях, этот газ применяется практически везде – начиная с приготовления еды на сковороде, и заканчивая резкой толстого слоя металла, активным использованием его на различных производствах вообще.
Также им все чаще заправляют свои автомобили люди, отказавшиеся от топлива на бензиновой основе.
Химические свойства бутана:
Бутан трудно вступает в химические реакции. В обычных условиях не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде.
Химические свойства бутана аналогичны свойствам других представителей ряда алканов. Поэтому для него характерны следующие химические реакции:
- 1. каталитическое дегидрирование бутана:
CH3-CH2-CH2-CH3 → CH2=CH-CH2-CH3 + H2 (kat = Pt, Ni, Al2O3, Cr2O3, повышенная to).
- 2. галогенирование бутана:
CH3-CH2-CH2-CH3 + Br2 → CH3-CHBr-CH2-CH3 + HBr (hv или повышенная to);
CH3-CH2-CH2-CH3 + I2 → CH3-CHI-CH2-CH3 + HI (hv или повышенная to).
Реакция носит цепной характер. Молекула брома или йода под действием света распадается на радикалы, затем они атакуют молекулы бутана, отрывая у них атом водорода, в результате этого образуется свободный бутил CH3-CH·-CH3, который сталкиваются с молекулами брома (йода), разрушая их и образуя новые радикалы йода или брома:
Br2 → Br·+ Br· (hv); – инициирование реакции галогенирования;
CH3-CH2-CH2-CH3 + Br· → CH3-CH·-CH2-CH3 + HBr; – рост цепи реакции галогенирования;
CH3-CH·-CH2-CH3 + Br → CH3-CHBr-CH2-CH3 + Br·;
CH3-CH·-CH2-CH3 + Br· → CH3-CHBr-CH2-CH3; – обрыв цепи реакции галогенирования.
Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование бутана проходит поэтапно – за один этап замещается не более одного атома водорода.
CH3-CH2-CH2-CH3 + Br2 → CH3-CHBr-CH2-CH3 + HBr (hv или повышенная to);
CH3-CHBr-CH2-CH3 + Br2 → CH3-CBr2-CH2-CH3 + HBr (hv или повышенная to);
и т.д.
Галогенирование будет происходить и далее, пока не будут замещены все атомы водорода.
- 3. нитрование бутана:
См. нитрование этана.
- 4. окисление (горение) бутана:
При избытке кислорода:
2C4H10 + 13O2 → 8CO2 + 10H2O.
При нехватке кислорода вместо углекислого газа (СО2) получается оксид углерода (СО), при еще меньшем количестве кислорода выделяется мелкодисперсный углерод сажа (в различном виде, в т.ч. в виде графена, фуллерена и пр.) либо их смесь.
- 5. сульфохлорирование бутана:
C4H10 + SO2 + Cl2 → C4H9-SO2Cl + … (hv).
- 6. сульфоокисление бутана:
2C4H10 + 2SO2 + О2 → 2C4H9-SO2ОН (повышенная to).
Основные физико-химические свойства компонентов СУГ и продуктов их сгорания
К основным характеристикам СУГ относят:
- температуру испарения/конденсации;
- температуру воспламенения;
- теплоту сгорания;
- плотность;
- объемное расширение.
Важными характеристиками являются пределы взрываемости при смешении с воздухом, быстрота распространения огня при горении, условия для полного сгорания.
Температура испарения/конденсации
При нормальном давлении составляет:
- для пропана – минус 42 °C;
- для бутана – минус 0,5 °C.
Если температура газов поднимается выше этих значений, они начинают испаряться, при опускании ниже – конденсироваться. Как правило, сжиженный газ поставляется в форме смеси (бутан+пропан). Поэтому фактическая температура испарения/конденсации зависит от их соотношения.
Обычно газ, поставляемый зимой, сохраняет испаряемость до минус 20 °C. Но иногда производитель поставляет смесь с повышенным количеством бутана. Это приводит к тому, что даже при небольшом понижении температуры ниже нуля газ перестает испаряться.
Температура воспламенения
Она равна:
- для пропана – от 504 до 588 °C;
- для бутана – от 430 до 569 °C.
При этих значениях температуры газ может воспламениться даже при отсутствии открытого огня – если имеются предметы, которые нагреты до высокой температуры, но еще не светятся.
Теплота сгорания
Этот параметр характеризует количество тепла, выделяемое при сгорании 1 м3 газа. Он равен:
- для пропана – 22…24 тыс. ккал. (91…99 МДж/ м3);
- для бутана – 28…31 тыс. ккал. (118…128 МДж/ м3).
Пределы взрываемости
Это очень важная с точки зрения безопасности характеристика. При определенном соотношении смесь газов с воздухом или кислородом может взрываться. Вероятность взрыва зависит от скорости распространения огня. Чем она выше, тем опаснее ситуация. В свою очередь скорость распространения огня зависит от пропорции газов. Нужно иметь в виду, что при увеличении температуры границы взрываемости расширяются.
При смешении газа с воздухом он становится взрывоопасным при следующих соотношениях:
- пропан – 2,1%…9,5%;
- бутан – 1,5%…8,5%;
- смесь – 1,5%…9,5%.
Плотность
Плотность газообразной фазы в норме составляет:
- пропана – 2,019 кг/ м3;
- бутана – 2,703 кг/ м3.
Плотность жидкой фазы – 0,5…0,6 кг/л.
Как видим, пары СУГ весят больше воздуха, плотность которого равна 1,29 кг/м3. Это приводит к тому, что при утечках газ собирается внизу помещения, где в относительно малом количестве может образовать с воздухом взрывоопасную смесь. Визуально это может быть похоже на дымку или стелющийся туман. При утечках из подземных коммуникаций и емкостей СУГ заполняют непроветриваемые углубления, подвалы, канализационные колодцы и остаются там довольно долго. Визуально обнаружить утечки трудно. Не выходя на поверхность, они растекаются под землей на довольно большие расстояния.
Объемное расширение
Объемное расширение жидкой фазы в 16 раз выше, нежели у воды. Это создает опасность разрыва баллона при увеличении температуры.
Степень сгораемости
Чтобы газ сгорал полностью, на 1 м3 его паров должно приходиться:
- для пропана – 24 м3 воздуха или 5,0 м3 О2;
- для бутана – 31 м3 воздуха или 6,5 м3 О2.
При испарении 1 кг жидкого газа образуется:
- пропана – 0,51 м3 паров;
- бутана – 0,386 м3 паров.
При испарении 1 л газа образуется:
- пропана – 0,269 м3 паров;
- бутана – 0,235 паров м3.
Скорость распространения огня
Пламя горящего бутана распространяется с максимальной скоростью 0,826 м/сек, пропана – 0,821 м/сек.
Цвет и запах
Чистые СУГ бесцветны и лишены запаха. Это создает опасность неконтролируемых утечек с последующим образованием взрывоопасных смесей. Чтобы облегчить своевременное обнаружение утечек, СУГ подвергают одоризации (приданию запаха) техническим этилмеркаптаном.
Назначение газа бутана
Несмотря на широкое распространение электроприборов, все еще не теряют своей актуальности газовые инструменты и оборудование. Паяльные лампы, газовые горелки, газовые паяльники, фонари, туристические плиты — эти и многие другие приборы пользуются большой популярностью и их продажи со временем только растут. Причина тому проста: газовые приборы мобильны, очень просты в работы и надежны, их можно использовать вдали от электросетей и цивилизации вообще.
Однако для работы таких приборов и инструментов необходим горючий газ, дающий пламя с высокой температурой. Сегодня для этой цели чаще других используется бутан в баллонах малого объема.
Бутан — газ бытового применения, который может использоваться для работы различных устройств, приборов, оборудования и инструментов:
- Зажигалки;
- Газовые паяльники;
- Газовые горелки (в том числе и лабораторные);
- Паяльные лампы;
- Мобильные газовые плиты (туристические);
- Газовые фонари.
Чтобы обеспечить нормальную работу всех этих устройств, необходимо знать о существующих типах и особенностях газов, а также правильно их подбирать.
Химические и физические свойства
Пропан-бутан обладает уникальнейшими химическими, физическим свойствами, что буквально и сделало его столь популярным среди потребителей всего мира.
Во-первых, этот представитель сжиженных углеродных газов остается в жидкой форме исключительно при большом давлении, которое равно 16-ти атмосферам. Поэтому при транспортировке вещество перевозят только в газовых баллонах с соответствующим давлением.
Температура горения пропана не равна какому-то определенному числу и колеблется в пределах между 800-1970 градусов по Цельсию. Столь высокие показатели полностью оправдывают ту пользу, которую он приносит в быту человека, ведь горение этой смеси имеет большой КПД при исполнении любых задач, связанных с использованием данного газа.
Температура кипения пропана составляет -42 градуса по Цельсию, что свидетельствует о гарантии безопасности эксплуатации в нормальных условиях.
Но так как мы рассматриваем смесь пропана с бутаном, то эта цифра может подняться до отметки -25 градусов и даже выше, в зависимости от процентного соотношения составляющих в веществе. Стоит учесть, что пропан замерзает при температуре -188 градусов.
При перевозке вещества не стоит забывать о температуре пропана в баллоне, которая не должна превышать отметку выше 15 градусов по Цельсию.
Такой подход считается наиболее безопасным, поскольку при транспортировке с высшей температурой газовых баллонов, существенно возрастает риск возгорания.
Кстати, что касается температуры воспламенения пропана-бутана, то и здесь они отличаются – у первого она составляет 504 градуса по Цельсию, а у второго – 430. Но, не смотря на столь большое количество отличий между своими составляющими, этот представитель сжиженных углеродных газов вполне конкурентный с бензиновыми горючими смесями.
Сфера применения газа
Пропан-бутан представляет собой уникальное вещество на газовой основе, которое имеет в своем составе одноименные молекулы.
Общепризнанная химическая формула пропана состоит из молекул и атомов двух основных составляющих – пропана (С3Н8) и бутана (С4Н10).
Широко используемый в бытовых целях, этот газ применяется практически везде – начиная с приготовления еды на сковороде, и заканчивая резкой толстого слоя металла, активным использованием его на различных производствах вообще.
Также им все чаще заправляют свои автомобили люди, отказавшиеся от топлива на бензиновой основе.

Эффекты и проблемы со здоровьем [ править ]
Вдыхание бутана может вызвать эйфорию , сонливость , потерю сознания , асфиксию , сердечную аритмию , колебания артериального давления и временную потерю памяти при злоупотреблении непосредственно из контейнера под высоким давлением и может привести к смерти от удушья и фибрилляции желудочков . Он попадает в кровоток и в течение нескольких секунд вызывает интоксикацию. Бутан является наиболее распространенным летучим веществом в Великобритании и был причиной 52% смертей, связанных с растворителями, в 2000 году. Распыляя бутан прямо в горло, струя жидкости может быстро охладиться до -20 ° C (-4 ° F) за счет расширения, вызывая длительный ларингоспазм . Синдром », впервые описанный Бассом в 1970 г. является наиболее частой причиной смерти, связанной с растворителями, приводя к 55% известных смертельных случаев.
Пропорции газов
Для топливной смеси бутан является более калорийным топливом, а пропан выступает в качестве сжиженного газа, который испаряется при низких температурах. Поэтому соотношение пропана и бутана в смеси зависит от климатических условий региона, в которых пропан-бутан используется, а также времени года.
Чем ниже температура, тем больше пропана должно быть в смеси (не менее 70—80%), тогда пропан обеспечит наилучшее испарение газа и, следовательно, топливо будет стабильно и надежно подаваться к потребителю.
А вот летом можно использовать смесь с содержанием пропана, не превышающим 40%
Если вы набираете топливо летом, а использовать его планируете зимой, то обратите свое внимание на газ с 60-70-процентным содержанием пропана
Польза и вред
Добавка E 943a по степени влияния на здоровье отнесена к малоопасным веществам (4 класс в соответствии с ГОСТ 12.1.007-76).
Бутан — нейтральный продукт, он не всасывается в кровь, не вступает в какие-либо химические реакции.
Серьезную опасность представляет непосредственное вдыхание газа. Бутан быстро вытесняет воздух. У пострадавшего отмечают признаки кислородной недостаточности:
- удушье,
- аритмию,
- резкое повышение артериального давления;
- возникновение очагов острой эмфиземы легких;
- потерю сознания.
Наркотическое действие, приписываемое «газу из зажигалок», учеными не доказано.
Получение бутана. Химические реакции – уравнения получения бутана:
Так как бутан в достаточном количестве содержится в природном газе, попутном нефтяном газе и выделяется при крекинге нефтепродуктов, его не получают искусственно. Его выделяют при очистке и сепарации из природного газа, ПНГ и нефти при перегонке.
Бутан в лабораторных условиях получается в результате следующих химических реакций:
- 1. гидрирования непредельных углеводородов, например, бутена:
CH3-CH2-CH=CH2 + H2 → CH3-CH2-CH2-CH3 (kat = Ni, Pt или Pd, повышенная to).
- 2. восстановления галогеналканов:
C4H9I + HI → C4H10 + I2 (повышенная to);
C4H9Br + H2 → C4H10 + HBr.
- 3. взаимодействия галогеналканов с металлическим щелочным металлом, например, натрием (реакция Вюрца):
2C2H5Br + 2Na → CH3-CH2-CH2-CH3 + 2NaBr;
2C2H5Cl + 2Na → CH3-CH2-CH2-CH3 + 2NaCl.
Суть данной реакции в том, что две молекулы галогеналкана связываются в одну, реагируя с щелочным металлом.
- 4. щелочного плавления солей одноосновных органических кислот:
C4H9-COOH + NaOH → C4H10 + Na2CO3 (повышенная to);
C4H9-COONa + NaOH → C4H10 + NaHCO3.
Получение — бутан
Получение бутанов даже путем трехступенчатого разделения может составлять 10 — 25 % дебита получаемого газа, при усло — — вии, что он не отбирается на экстракционной установке.
Получение бутанов даже путем трехступенчатого разделения может составлять 10 — 25 % дебита получаемого газа, при условии, что он не отбирается на экстракционной установке.
Описано также получение бутана.
Установка служит для получения бутана, пропана и пропилена из газов каталитического крекинга.
Так как источником получения бутана является нефть, а основная масса добываемых в СССР нефтей относится к классу сернистых31, целесообразно изучить влияние на процесс окисления бутана сернистых соединений.
Укажите по три способа получения бутана и 2 4-диме-тилпентана.
Укажите по три способа получения бутана и 2 4-диметилпентана.
Укажите по три способа получения бутана и 2 4-диме-тилпентана.
|
Ионизационная камера для измерения 3-излучения газов. |
К сожалению, из-за образования побочных продуктов потери активности достигают 50 % исходной, поэтому условия реакции приходится подбирать таким образом, чтобы был достигнут теоретический выход по газу и исключался изотопный эффект. В пользу получения бутана реакцией воды с бутилмагнийбромидом говорят два соображения: получается химически чистый газ ( исходный продукт можно приготовить очень чистым) и бутан можно быстро и количественно выморозить жидким азотом. Для измерения используется ионизационная камера ( см. раздел 10), которая по сравнению с пропорциональным счетчиком и счетчиком Гейгера — Мюллера нечувствительна к загрязнениям газа и влажности. Поэтому отпадает требующая много времени откачка системы диффузионным насосом для удаления примесей, особенно кислорода. В отличие от счетных трубок ионизационная камера позволяет измерять как очень малые, так и очень большие активности. К выбору типа ионизационной камеры не предъявляется особенных требований. Обычно применяются камеры из хромированной латуни или меди емкостью 250 или 500 мл.
В результате получается стабильная нефть, отправляемая далее на нефтеперерабатывающие заводы, и широкая фракция низкокипящих углеводородов ( газы стабилизации), представляющая собой смесь сжиженных газов и легкого бензина. Это основной источник сырья для получения бутана, изобутана, пентана и изо-пентана.
Катализаторы на основе фтористого бора способствуют реакциям расщепления парафиновых углеводородов с последующим уплотнением. Этот же катализатор рекомендуется для получения бутанов из пропана и пентана , а также из пентанов углеводородов, соответствующих бензинам.
Основным сырьем для производства технического изооктана, иначе называемого алкилатом, являются бутаны, которые получаются в значительных количествах при процессе гидрогенизации тверых и жидких высокомолекулярных продуктов. Выход бутанов увеличивается при производстве ароматизированного бензина из бензинов гидрогенизации или при специальных режимах получения бутанов как целевых продуктов, о чем уже ранее говорилось.
Выход бутанов увеличивается при производстве ароматизированного бензина из бензинов гидрогенизации или при специальных режимах получения бутанов как целевых продуктов ( см. гл.
Основными источниками производства непредельных углеводородов С4 в нашей стране являются вторичные процессы переработки нефти и целенаправленного дегидрирования бутанов, выделяемых из нефтяных попутных газов и газов нефтестабилизации. Однако объем получаемых на нефтеперерабатывающих заводах бутиленовых фракций не — может полностью удовлетворить растущую потребность промышленности основного органического синтеза и производства высококачественного моторного топлива. Недостаточные темпы получения бутанов из газов нефтедобычи сдерживают развитие производства бутиленов и дивинила в процессах каталитического дегидрирования этих углеводородов.
Использует
Обычный бутан можно использовать для бензин смешивание в качестве топливного газа растворителя для экстракции ароматизаторов, отдельно или в смеси с пропан, и как сырье для производства этилен и бутадиен, ключевой ингредиент синтетическая резина. Изобутан в основном используется нефтеперерабатывающие заводы для усиления (увеличения) октан количество автомобильного бензина.
При смешивании с пропан и других углеводородов, он может называться коммерчески СУГ, для сжиженного углеводородного газа. Используется как компонент бензина, как сырье для производства базовых нефтехимия в паровой крекинг, как топливо для сигарет зажигалки и как пропеллент в аэрозоли Такие как дезодоранты.
Очень чистые формы бутана, особенно изобутана, могут использоваться в качестве хладагенты и в значительной степени заменили разрушающий озоновый слой галометаны, например, в бытовых холодильниках и морозильниках. Рабочее давление системы для бутана ниже, чем для галометанов, таких как R-12Таким образом, системы с R-12, такие как автомобильные системы кондиционирования воздуха, при преобразовании в чистый бутан не будут работать оптимально, и поэтому используется смесь изобутана и пропана для обеспечения производительности системы охлаждения, сравнимой с R-12.
Бутан также используется как более легкий топливо для обычной зажигалки или бутановая горелка и продается в бутылках в качестве топлива для приготовления пищи, барбекю и походных печей. На мировом рынке канистр с бутаном доминируют южнокорейский производители.
В качестве топлива его часто смешивают с небольшими количествами сероводород и меркаптаны что придаст несгоревшему газу неприятный запах, который легко уловить человеческим носом. Таким образом можно легко определить утечку бутана. Хотя сероводород и меркаптаны токсичны, они присутствуют в таких низких количествах, что опасность удушья и возгорания бутаном становится проблемой задолго до токсичности.[нужна цитата] Наиболее коммерчески доступный бутан также содержит определенное количество загрязняющего масла, которое можно удалить путем фильтрации, но которое в противном случае оставит отложение в точке воспламенения и может в конечном итоге заблокировать равномерный поток газа.Загрязняющие вещества не используются при экстракции ароматизаторов.[уточнить] и бутановые газы могут вызвать взрыв газа в плохо вентилируемых помещениях, если утечки остаются незамеченными и воспламеняются от искры или пламени.[нужна цитата]
| Канистры бутанового топлива для использования в походных печах. | Бутановая зажигалка с резервуаром для жидкого бутана | Аэрозольный баллончик, в котором в качестве пропеллента может использоваться бутан. | Баллон с бутаном, используемый для приготовления пищи |